Pojemność cieplna - stosunek ilości
ciepła
(dQ) dostarczonego do układu, do odpowiadającego mu przyrostu
temperatury
(dT).

gdzie:
- C - pojemność cieplna
- Q - ciepło
- T - temperatura
Pojemność cieplna przypadająca na jednostkę masy to
ciepło właściwe
a na 1
mol
to
molowe ciepło właściwe
(ciepło molowe).
Pojemność cieplna C jest związana z ciepłem właściwym poprzez zależność:
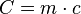
gdzie:
- c - ciepło właściwe
- m - masa substancji
Pojemność cieplną z molowym ciepłem właściwym wiąże zależność:

gdzie:
W wszystkich równaniach poniżej użyta jest molowa pojemność cieplna.
Pojemność cieplna gazów
W przypadku układów zawierających fazy nieskondensowane (
gazy
i
pary
) często konieczne jest jeszcze rozróżnienie warunków, w których określana jest (molowa) pojemność cieplna:
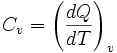

Ciepło absorbowane przez gaz powoduje wzrost energii kinetycznej cząsteczek tego gazu. Zgodnie z
zasadą ekwipartycji energii
, energia kinetyczna cząsteczki rozkłada się równo na wszystkie stopnie swobody. W związku z tym pojemność cieplna będzie zależała od liczby stopni swobody cząsteczki gazu i. Dla pojemności cieplnej przy stałej objętości obowiązuje

- gdzie R jest
stałą gazową
.
Dla jednoatomowego
gazu doskonałego
, gdzie
energia wewnętrzna
składa się jedynie z
energii kinetycznej
ruchu postępowego
cząsteczek
:

Dla gazów składających się z cząsteczek wieloatomowych, pojemność cieplna zależy od ich budowy, gdyż oprócz ruchu postępowego cząsteczek występuje także ruch obrotowy. Dla gazu dwuatomowego, możliwy jest wzrost energii cząsteczek poprzez
obrót
wokół 2 prostopadłych do siebie osi, skąd:

Cząsteczki gazu wieloatomowego może absorbowaną energię wykorzystać do obrotów wokół 3 różnych prostopadłych osi:

Pojemność molowa przy stałej objętości i pojemność molowa przy stałym ciśnieniu są powiązana ze sobą następującą zależnością:
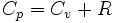
Pojemność przy stałym ciśnieniu jest większa, ponieważ gdy ciepło jest dostarczane, a ciśnienie jest stałe, wówczas gaz wykonuje pracę, na co zużywa część energii dostarczonej w postaci ciepła.
Z powyższej zależności wynika wzór na pojemność cieplną przy stałym ciśnieniu:

I tak na przykład dla gazu jednoatomowego:

W przypadku złożonych cząsteczek, oprócz stopni swobody związanych z ruchami translacyjnymi i z rotacją mogą wystąpić również oscylacyjne stopnie stopnie swobody, związane ze względnymi drganiami elementów cząsteczki. Wówczas liczba stopni swobody może rosnąc wraz ze wzrostem liczby atomów w cząsteczce.