|
|
Aktualna kategoria:
Nauka » Chemia » Liceum - lekcje
| 1 | | | 2 | | | 3 | | | 4 | | | 5 | | | 6 | | | 7 | | | 8 | | | 9 | | | 10 | | | 11 | | | 12 | | | 13 | | | 14 | | | 15 | | | 16 | | | 17 | | | 18 | | | ... | | | 25 | | | 26 | |
|
|
|
Elektroliza wodnych roztworów kwasów
Kwasy beztlenowe
Stężenie jonów wodorowych maleje, więc pH roztworu wzrasta
HCl K(-) : 2H + +2e --> H 2; A (+) 2Cl - -- > Cl 2 + 2e
Sumarycznie : 2HCl -- > H2 + Cl2
Kwasy tlenowe
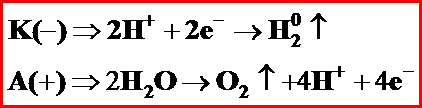
|
H2SO4 -- >2H+ + SO42-
K(-) 2H+ + 2e -- > H2↑ ; A (+) H2O – 2e ->1/2 O2 + 2H+
Sumarycznie: H2O -> H2 + ½ O2
|

|
A (+) Stężenie jonów wodorowych wzrasta, więc pH maleje
|
|
|
|
|
Pobierz lekcję
|
Udostępnij link do tej lekcji innym uczniom:
|
|