Do porównania mocy elektrolitów Arrhenius wprowadził pojęcie
stopnia i stałej dysocjacji elektrolitycznej.
Stopień dysocjacji α określa, jaka część wprowadzonych do roztworu cząsteczek uległa dysocjacji.
Matematycznie wyraża się wzorami:
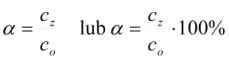
gdzie:
α – stopień dysocjacji
c
z – ilość moli cząsteczek, które uległy dysocjacji(stężenie molowe cząsteczek zdysocjowanych)
c
0 – ogólna ilość moli cząsteczek w roztworze (stężenie molowe roztworu)
W zależności od stopnia dysocjacji w roztworach 0,1 molowych elektrolity dzielimy:
elektrolity mocne – α zawiera się w przedziale 30% – 100%
elektrolity średnie –α zawiera się w przedziale 5% – 30%
elektrolity słabe – α zawiera się w przedziale 0% – 5%